이 논문은 편도체–시상하부–간 축이 어떻게 급성 스트레스 상황에서 신속하게 대사 변화를 유도하는지를 밝힌 연구다. 기존 교과서적 스트레스 시스템(HPA축, 부신수질)과는 별개의 새로운 신경회로가, 스트레스 유발 시 혈당 상승과 식욕 억제 등 중요한 생리적 변화를 조절함을 보여준다. 반복적 스트레스를 받으면 이 경로의 기능이 저하되며, 이는 2형 당뇨병 등 대사질환과 연관될 수 있다는 점을 시사한다.
1. 스트레스와 에너지 동원: 기존 지식
동물이 위협이나 스트레스 상황에 처하면, 신체는 에너지 저장소를 신속히 동원하여 도망치거나(도피), 얼어붙거나(동결) 등의 방어 행동에 필요한 체력을 확보한다. 이 과정에서 심혈관, 근육계 반응이 활성화되고, 당 대사 변화도 나타난다. 예를 들어,
"스트레스에 대한 혈당 반응은 '투쟁-도피' 행동과 밀접하게 연관되어 있다."
이처럼 혈당 상승(고혈당)은 기억력이나 상황 판단력도 높여, 위협을 신속하게 분석할 수 있도록 도와준다. 한편, 먹이나 탐색 등 방어와 경쟁하는 행동은 억제된다. 이런 대사적 긴급 적응력은 진화적으로 보존되어 왔으며, 중요함에도 불구하고 이런 반응을 조율하는 뇌 회로에 대한 이해는 아직 부족하다.
2. 새로운 편도체–간 신경회로 발견
연구진은 새로운 '편도체–시상하부–간(AMG-VMH-Liver)' 축을 규명했다. 이 축은 기존의 HPA축, 부신수질과 독립적으로 스트레스 상황에서 혈당을 빠르게 올리고, 식욕을 억제하는 역할을 한다. 반복적 스트레스는 이 회로 기능을 저하시켜 2형 당뇨병 등 대사이상과 연계됨을 발견했다.
3. 스트레스가 대사에 미치는 변화
C57Bl/6 생쥐를 '급성 속박 스트레스', '사회적 스트레스(다른 수컷이 점유한 케이지 냄새)'에 노출시키면 즉각적으로 혈당이 상승하고 식욕이 억제되는 것이 관찰되었다.
- 이 과정에서 코르티코스테론, 아드레날린, 글루카곤 농도가 증가했지만, 인슐린, 노르아드레날린은 변화가 없었다.
- 스트레스가 간의 글루코스 생산 유전자(G6pc)의 발현을 늘리는 것도 확인.
- 5분만의 아주 짧은 스트레스에도 혈당과 스트레스 호르몬이 신속하게 상승했다.
"속박 스트레스는 혈중 포도당을 급격히 올리고, 식욕을 감소시켰다."
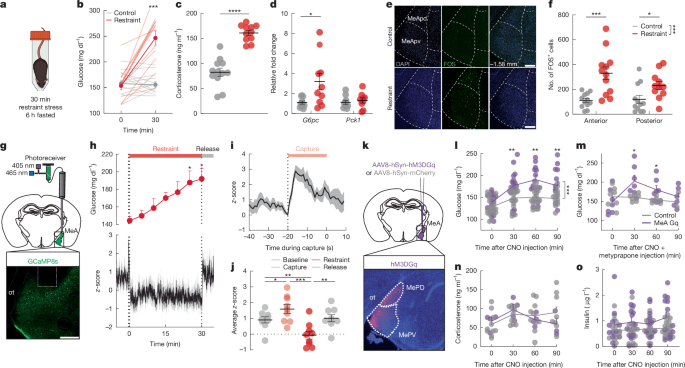
4. 편도체(MeA) 뉴런의 활성화와 기능
- 스트레스가 편도체(MeA) 뉴런의 활성을 유발했다.
- 실시간 칼슘 이미지를 통해, 위협상황이 시작되기 전 '포획' 순간에 MeA 뉴런이 급격히 활성화됨을 보여줌.
- 이 활성은 혈당 증가보다 앞서 나타난다.
- DREADD(화학유전적) 기법으로 MeA 뉴런을 인위적으로 흥분시키면,
- 스트레스를 주지 않아도 혈당이 상승함
- 기존 스트레스 축(HPA, 부신수질) 호르몬 없이도 혈당을 올릴 수 있음을 확인
"편도체(MeA) 활성화만으로도, 별도의 호르몬 변화 없이 혈당을 올릴 수 있었다."
이 효과는 식욕 억제 역시 유발했으며, 불안 및 공포 관련 행동과는 직접적 관련이 없었다.
5. 세부 회로: MeA→VMH와 MeA→BNST
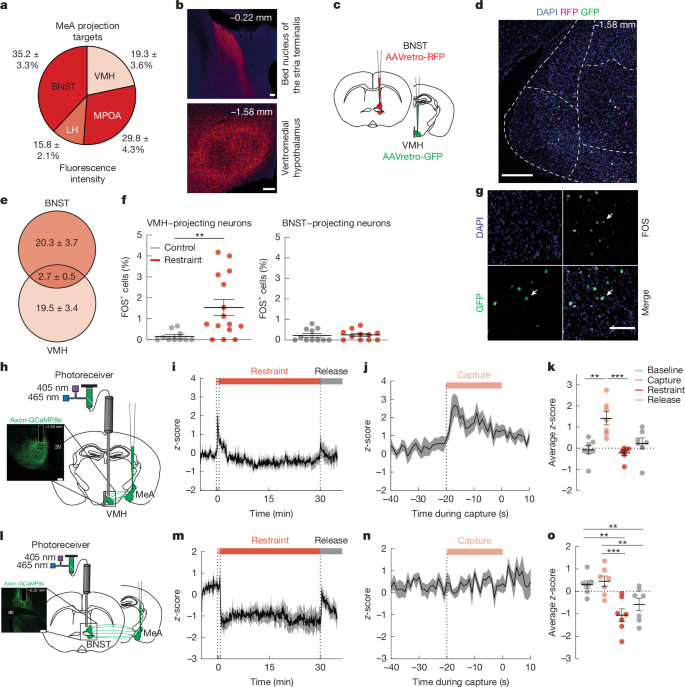
- MeA에서 시상하부의 복내측핵(VMH), BNST로 각각 신경다발이 이어진다.
- 스트레스 상황에서는 특히 MeA→VMH 뉴런만이 활발히 활성화되어 혈당 상승에 관여함이 확인되었다.
- MeA→BNST 회로는 스트레스에 관련된 다른 역할이 있으나, 혈당 조절에는 실질적 관여가 적음.
"급성 스트레스는 MeA→VMH 뉴런을 일차적으로 활성화시킨다."
6. 다양한 뉴런 집단의 참여와 기능 유전자
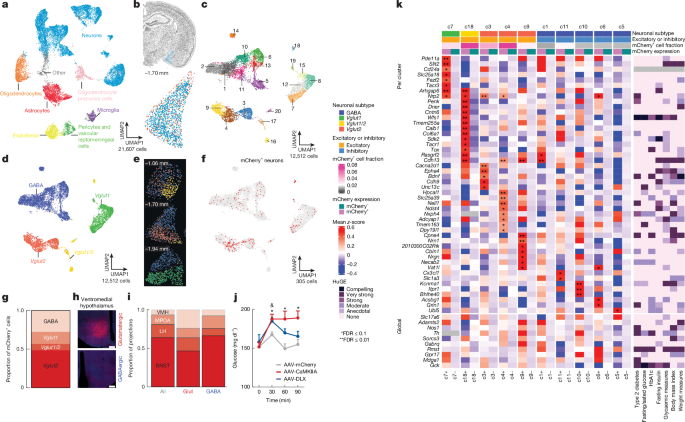
- MeA→VMH 경로에는 글루탐산성(흥분성)과 GABA성(억제성) 뉴런 모두가 속한다.
- 이들 뉴런은 간 신호 조절과 연관된 유전자(G6pc 등)의 발현에서 차이점을 나타냄.
- 유전자 수준에서 사람의 혈당, 체중, 당뇨와 관련된 변화와도 연관성이 있음.
"MeA→VMH 경로는 흥분성/억제성 뉴런 모두가 혈당상승에 기여한다."
7. MeA–VMH 회로의 직접적 간 조절 메커니즘
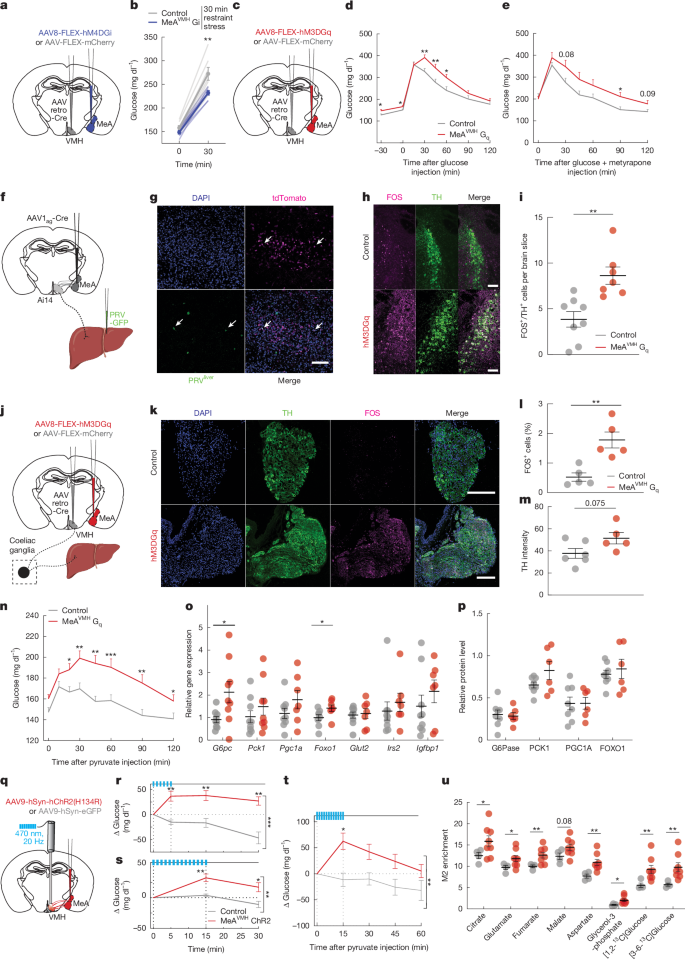
- MeA→VMH 뉴런을 차단하면, 스트레스 상황에서 고혈당 반응이 잘 나타나지 않음.
- 반대로 해당 뉴런을 활성화하면 혈당이 오르고, 이 작용은 인슐린, 글루카곤, 코르티코스테론 등 '고전적 호르몬'과 무관하다.
- 간으로 신경 경로가 이어져 있어, VMH에서 말초로 sympathetic(교감신경)을 통해 간에서 포도당 생산(신생합성)을 촉진함이 확인됨.
- PRV-GFP 바이러스와 Cre-tracing으로 다단계 신경 연결이 직접적으로 밝혀짐.
- 실제로 이 회로를 강제 자극하면, 간에서 포도당 신생합성 관련 유전자와 대사 과정이 신속히 활성됨
- 이 신경 회로는 간의 글루코스 생산 증가 → 혈당 상승 → 방어 행동 뒷받침 흐름을 만든다.
"편도체-시상하부-간 회로는 간에서 포도당 생산을 증가시켜 스트레스 대처를 돕는다."
8. 반복적 스트레스의 회로 마비와 대사질환 위험
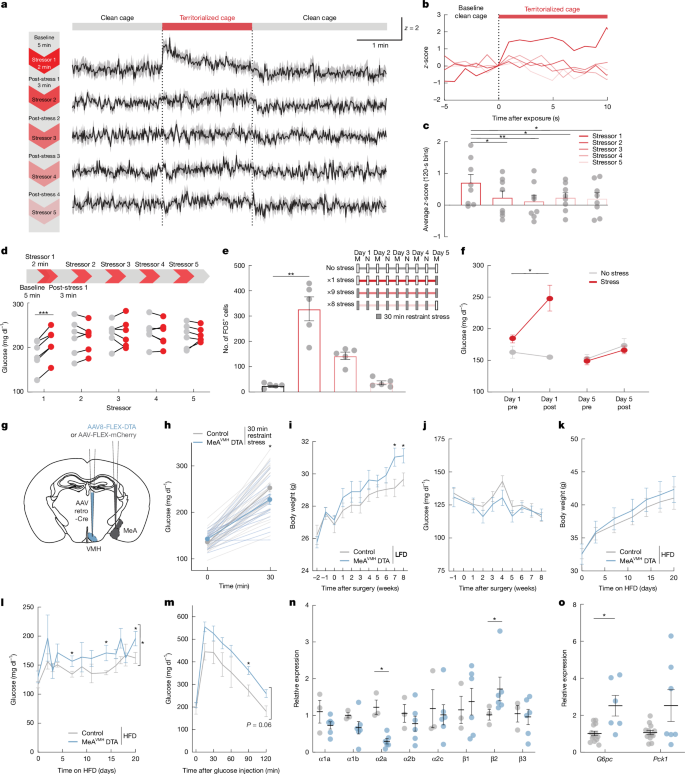
- 여러 차례 스트레스를 반복하면(예: 반복적 속박 또는 사회적 스트레스)
- 처음엔 혈당/뉴런활성도 크게 증가, 이후는 반복 노출 시 뉴런 활성화·혈당 반응이 점차 저하됨(마비 현상)
- 실험적으로 MeA→VMH 뉴런을 고갈시키면
- 스트레스에 따른 혈당 상승이 줄고
- 높은 지방식 등 대사적 부담 상황에서 혈당 조절 악화, 체중 증가, 간의 대사 유전자 발현 이상이 심해졌다
- 즉, 만성적 스트레스 또는 이 회로의 장애는 대사질환(비만, 2형 당뇨 등) 위험성 증가와 맞닿아 있다.
"반복 스트레스에 익숙해진 뒤, 이 회로의 기능 마비가 대사장애와 체중 증가를 유발한다."
9. 결론: 뇌-간 회로에서 보는 스트레스와 대사질환 연계 🌱
본 연구는 편도체–시상하부–간 회로라는, 고전적 호르몬축과 독립적으로 급성 스트레스 반응에서 대사(특히 혈당 조절)를 조율하는 신경경로를 밝혔다는 점에서 의의가 크다.
이 회로의 반복적 마비는 지속적 고혈당과 대사질환 악화로 이어질 수 있어, 스트레스 관리가 대사질환 예방 관점에서도 중요함을 시사한다.
"만약 인간에서도 이러한 메커니즘이 작동한다면, 만성 스트레스 노출자에서 편도체 신호 이상이 대사질환 위험 증가로 이어질 수 있다."
마무리
이 논문은 우리가 스트레스를 받을 때 왜 혈당이 오르고, 왜 만성 스트레스가 당뇨나 비만 등 질환 위험을 높일 수 있는지를 뇌와 간의 신경 회로 관점에서 새롭게 설명해준다. 뇌–신체–대사 연결고리를 이해하는 데 중요한 단서를 제공하며, 스트레스 대처와 대사질환 예방을 통합적으로 접근할 필요가 있음을 강조한다. 😊